آهک ساختمانی: خواص و کاربرد. آهک سریع
کاربرد آن.
آهک خرد شده(فرمول - Ca(OH)2) یک پایه قوی است. ممکن است اغلب در برخی منابع تحت نام هیدروکسید کلسیم یا "کرک" یافت شود.
خواص:این به صورت پودر سفید رنگی است که کمی در آب محلول است. هر چه دمای محیط کمتر باشد، حلالیت آن کمتر است. محصولات واکنش آن با اسید نمک های کلسیم مربوطه هستند. به عنوان مثال، غوطه ور کردن آهک در اسید سولفوریک باعث تولید سولفات کلسیم و آب می شود. اگر محلول کرکی را در هوا بگذارید، با یکی از اجزای دومی - دی اکسید کربن - تعامل خواهد داشت. در این فرآیندمحلول کدر می شود محصولات این واکنش کربنات کلسیم و آب است. اگر به حباب زدن ادامه دهید دی اکسید کربن، واکنش با تشکیل بی کربنات کلسیم به پایان می رسد که با افزایش دمای محلول از بین می رود. آهک خرد شده و مونوکسید کربندر دمای حدود 400 درجه سانتیگراد برهمکنش خواهد داشت، محصولات آن کربنات و هیدروژن از قبل شناخته شده خواهد بود. این ماده همچنین می تواند با نمک ها واکنش دهد، اما تنها در صورتی که فرآیند با تشکیل رسوب به پایان برسد، به عنوان مثال، اگر "کرک" را با سولفیت سدیم مخلوط کنید، محصولات واکنش هیدروکسید سدیم و سولفیت کلسیم خواهند بود.
آهک از چه چیزی ساخته می شود:خود نام "کوئنچ" نشان می دهد که چیزی برای به دست آوردن این ماده خاموش شده است. همانطور که همه می دانند، هر ترکیب شیمیایی(یا اصلاً هر چیزی) معمولاً با آب خاموش می شود. و او چیزی برای واکنش به آن دارد. در شیمی ماده ای به نام آهک سریع وجود دارد. پس با افزودن آب به آن ترکیب مورد نظر به دست می آید.
کاربرد:آهک کنده شده برای سفید کردن هر اتاق استفاده می شود. همچنین برای نرم کردن آب استفاده می شود: اگر کرک را به بی کربنات کلسیم اضافه کنید، اکسید هیدروژن و یک رسوب نامحلول تشکیل می شود - کربنات فلز مربوطه. آهک آب شده در دباغی چرم، سوزاندن کربنات های سدیم و پتاسیم، به دست آوردن ترکیبات کلسیم، اسیدهای آلی مختلف و بسیاری از مواد دیگر استفاده می شود.
با استفاده از محلول "کرک" - آب آهک معروف - می توانید وجود دی اکسید کربن را تشخیص دهید: وقتی با آن واکنش می دهد، کدر می شود (عکس). دندانپزشکی نمی تواند بدون بحث هیدروکسید کلسیم کار کند، زیرا به لطف آن، در این شاخه از پزشکی می توان کانال ریشه دندان ها را ضد عفونی کرد. ملات آهک نیز با استفاده از آهک ژولیده از مخلوط کردن آن با ماسه ساخته می شود. مخلوط مشابهی در زمان های قدیم استفاده می شد ، سپس هیچ سنگ تراشی ساختمانی بدون آن نمی توانست انجام دهد. با این حال، در حال حاضر، به دلیل آزاد شدن غیر ضروری آب در هنگام واکنش کرک با ماسه، این محلول با موفقیت با سیمان جایگزین شده است. از هیدروکسید کلسیم برای تولید کودهای آهک استفاده می شود، همچنین یک افزودنی غذایی E526 است... و بسیاری از صنایع دیگر بدون استفاده از آن نمی توانند کار کنند.
آهک سریع – آهک زنده (اکسید کلسیم تصفیه نشده) از کلسینه کردن سنگ آهک حاوی خاک رس بسیار کم یا بدون خاک تولید می شود. خیلی سریع با آب ترکیب می شود و مقدار قابل توجهی گرما آزاد می کند و آهک خشک شده (هیدروکسید کلسیم) را تشکیل می دهد.
آهک دارای خواص مفید بسیاری است، به همین دلیل آن را پیدا می کند کاربرد گستردهدر ساخت و ساز، صنعت کشاورزی.
خواص:قطعات ریز متخلخل CaO به اندازه 5…10 سانتی متر که پس از پختن مواد اولیه به دست می آیند. چگالی متوسط 1600…1700 کیلوگرم بر متر مکعب.
بسته به محتوای اکسید منیزیم، آهک هوا به کلسیم (70...90٪ CaO و تا 5٪ MO)، منیزیم (تا 20٪ Mg0) و منیزیم بالا یا دولومیت (Mg0 از 20 تا 40) تقسیم می شود. ٪.
آهک زنده در سه درجه تولید می شود. بسته به زمان خاموش شدن، همه انواع آهک متمایز می شوند: آهک سریع خاموش (زمان کند شدن تا 8 دقیقه). خاموش کردن متوسط (تا 25 دقیقه)، خاموش کردن آهسته (بیش از 25 دقیقه).
آهک هوایی ساختمانی به سه درجه تقسیم می شود.
چگالی آهک زنده بین 1/3 تا 3/3 گرم بر سانتیمتر مکعب است و عمدتاً به دمای پخت، وجود ناخالصیها، زیرسوختگی و بیشسوختگی بستگی دارد.
چگالی آهک هیدراته به درجه تبلور آن بستگی دارد و برای Ca(OH)2 برابر با 23/2 است که به صورت صفحات شش ضلعی متبلور شده و برای آهک آمورف 08/2 گرم بر سانتی متر مکعب است.
جرم حجمی کلوخه آهک زنده در
قطعه تا حد زیادی به دمای پخت بستگی دارد و از 1.6 گرم بر سانتی متر مکعب (آهک پخته شده در دمای 800 درجه سانتی گراد) به 2.9 گرم در سانتی متر مکعب (پخش طولانی مدت در دمای 1300 درجه سانتی گراد) افزایش می یابد.
جرم حجمی برای انواع دیگر آهک به شرح زیر است: برای آهک زنده آسیاب شده در حالت ریزش آزاد 900-1100، در حالت فشرده 1100-1300 کیلوگرم بر متر مکعب. برای آهک هیدراته (کرک) در حالت ریخته شده شل - 400-500، در حالت فشرده 600-700 کیلوگرم بر متر مکعب؛ برای خمیر آهک - 1300-1400 کیلوگرم در متر مکعب.
پلاستیسیته، که تعیین کننده توانایی بایندر در ایجاد کارایی به ملات و بتن است، مهمترین ویژگی آهک است. انعطاف پذیری آهک با ظرفیت بالای نگهداری آب آن مرتبط است. ذرات ریز پراکنده هیدرات اکسید کلسیم، جذب مقدار قابل توجهی آب روی سطح خود، نوعی روان کننده برای دانه های سنگدانه در ملات یا مخلوط بتن ایجاد می کند و اصطکاک بین آنها را کاهش می دهد. در نتیجه ملات آهکآنها کارایی بالایی دارند، به راحتی و به طور یکنواخت در یک لایه نازک بر روی سطح آجر یا بتن توزیع می شوند، به خوبی به آنها می چسبند و با قابلیت نگهداری آب حتی زمانی که روی آجر و سایر بسترهای متخلخل استفاده می شوند مشخص می شوند.
کاربرد:این ماده به طور گسترده در مناطق مختلف فعالیت انسانی. بزرگترین مصرف کنندگان عبارتند از: متالورژی آهنی، کشاورزی، شکر، صنایع شیمیایی، خمیر و کاغذ. CaO همچنین در صنعت ساخت و ساز استفاده می شود. اهمیت ویژهارتباط در زمینه اکولوژی وجود دارد. آهک برای حذف اکسید گوگرد از گازهای دودکش استفاده می شود. این ترکیب همچنین قادر است آب را نرم کند و محصولات و مواد آلی موجود در آن را رسوب دهد. علاوه بر این، استفاده از آهک زنده خنثی سازی اسیدهای طبیعی و فاضلاب. در کشاورزی، در تماس با خاک، این ترکیب اسیدی را که برای آن مضر است از بین می برد گیاهان کشت شده. آهک زنده خاک را با کلسیم غنی می کند. به همین دلیل قابلیت کشت زمین افزایش می یابد و پوسیدگی هوموس تسریع می یابد. در عین حال، نیاز به کودهای نیتروژن در دوزهای زیاد کاهش می یابد.
مخلوط هیدرات در پرورش طیور و دام برای تغذیه استفاده می شود. این باعث از بین رفتن کمبود کلسیم در رژیم غذایی می شود. علاوه بر این، این ترکیب برای بهبود شرایط عمومی بهداشتی هنگام نگهداری و پرورش دام استفاده می شود. در صنایع شیمیایی از آهک هیدراته و مواد جاذب برای تولید کلسیم فلوراید و هیدروکلراید استفاده می شود. در صنعت پتروشیمی، این ترکیب تارهای اسیدی را خنثی می کند و همچنین به عنوان یک معرف در سنتز معدنی و آلی بازی عمل می کند. آهک به طور گسترده در ساخت و ساز استفاده می شود. این به دلیل سازگاری بالای مواد با محیط زیست است. این مخلوط در تهیه مواد اتصال دهنده، بتن و ملات و تولید محصولات ساختمانی استفاده می شود.
خوردگی فلزات و روشهای حفاظت در برابر خوردگی
خوردگی فلز- فرآیند تخریب فلزات و آلیاژها در اثر برهمکنش شیمیایی یا الکتروشیمیایی با محیط خارجی که در نتیجه آن فلزات اکسید شده و خواص ذاتی خود را از دست می دهند. خوردگی دشمن است محصولات فلزی. هر ساله در جهان 10...15% فلز ذوب شده در اثر خوردگی یا 1...1.5% کل فلز انباشته شده و مورد بهره برداری انسان از بین می رود.
خوردگی شیمیایی- تخریب فلزات و آلیاژها در نتیجه اکسیداسیون هنگام برهم کنش با گازهای خشک در دمای بالایا با مایعات آلی - فرآورده های نفتی، الکل و غیره.
خوردگی الکتروشیمیایی- تخریب فلزات و آلیاژها در آب و محلول های آبی. برای ایجاد خوردگی کافی است که فلز به سادگی پوشانده شود نازک ترین لایهآب جذب شده (سطح مرطوب). به دلیل ناهمگونی ساختار فلز در هنگام خوردگی الکتروشیمیایی، جفت های گالوانیکی (کاتد - آند) در آن تشکیل می شود، به عنوان مثال، بین دانه های فلزی (کریستال ها) که از نظر ترکیب شیمیایی با یکدیگر متفاوت هستند. اتم های فلز از آند به شکل کاتیون وارد محلول می شوند. این کاتیون ها با ترکیب آنیون های موجود در محلول، لایه ای از زنگ را روی سطح فلز تشکیل می دهند. فلزات عمدتاً در اثر خوردگی الکتروشیمیایی از بین می روند.
خوردگی فلزات در نتیجه خوردگی خسارت اقتصادی زیادی ایجاد می کند، تجهیزات، ماشین آلات، مکانیزم ها از کار می افتند و از بین می روند سازه های فلزی. به ویژه در برابر خوردگی تجهیزات در تماس با محیط تهاجمیبه عنوان مثال محلول های اسیدها و نمک ها.
در شرایط عادیفلزات می توانند با مواد موجود در محیط - اکسیژن و آب وارد واکنش های شیمیایی شوند. لکه هایی روی سطح فلزات ظاهر می شود، فلز شکننده می شود و نمی تواند بارها را تحمل کند. این منجر به از بین رفتن محصولات فلزی می شود که تولید آنها صرف شده است تعداد زیادیمواد خام، انرژی و میزان تلاش انسان.
خوردگی عبارت است از تخریب خود به خودی فلزات و آلیاژها تحت تأثیر محیط زیست.
نمونه بارز خوردگی زنگ زدگی سطح فولاد و محصولات چدن. هر ساله حدود یک چهارم آهن تولید شده در جهان به دلیل خوردگی از بین می رود. هزینههای تعمیر یا تعویض کشتیها، وسایل نقلیه، ابزارآلات و ارتباطات، لوله های آبچندین برابر بیشتر از هزینه فلزی که از آن ساخته شده اند. محصولات خوردگی محیط زیست را آلوده کرده و بر زندگی و سلامت افراد تأثیر منفی می گذارد.
خوردگی شیمیایی در صنایع شیمیایی مختلف رخ می دهد. در اتمسفر گازهای فعال (هیدروژن، سولفید هیدروژن، کلر)، در محیط اسیدها، قلیایی ها، نمک ها و همچنین در نمک های مذاب و سایر مواد، واکنش های خاصی رخ می دهد. مواد فلزی، که از آن دستگاهی که فرآیند شیمیایی در آن انجام می شود ساخته می شود. خوردگی گاز در دماهای بالا رخ می دهد. اتصالات کوره و قطعات موتورهای احتراق داخلی تحت تأثیر آن قرار می گیرند. خوردگی الکتروشیمیایی زمانی اتفاق میافتد که فلز در هر کدام وجود داشته باشد محلول آبی.
بیشتر مواد فعالعوامل محیطی که بر روی فلزات اثر می کنند عبارتند از: اکسیژن O2، بخار آب H2O، کربن (IV) اکسید CO2، گوگرد (IV) اکسید SO2، نیتروژن (IV) اکسید NO2. فرآیند خوردگی در تماس فلزات با آب نمک بسیار تسریع می شود. به همین دلیل کشتی ها زنگ می زنند آب دریاسریعتر از آب شیرین
ماهیت خوردگی اکسیداسیون فلزات است. محصولات خوردگی می توانند اکسید، هیدروکسید، نمک و غیره باشند. به عنوان مثال، خوردگی آهن را می توان به صورت شماتیک با معادله زیر توصیف کرد:
4Fe + 6H2O + 3O2 → 4Fe (OH) 3.
جلوگیری از خوردگی غیرممکن است، اما می توان آن را کاهش داد. راه های زیادی برای محافظت از فلزات در برابر خوردگی وجود دارد، اما تکنیک اصلی جلوگیری از تماس آهن با هوا است. برای انجام این کار، محصولات فلزی رنگ شده، لاک زده یا با لایه ای از روان کننده پوشانده می شوند. در بیشتر موارد، این برای جلوگیری از خراب شدن فلز برای چندین ده یا حتی صدها سال کافی است. راه دیگری برای محافظت از فلزات در برابر خوردگی پوشش الکتروشیمیاییسطوح فلزی یا آلیاژی با سایر فلزات مقاوم در برابر خوردگی (آبکاری نیکل، آبکاری کروم، گالوانیزه، آبکاری نقره و آبکاری طلا). در فناوری اغلب از آلیاژهای ویژه مقاوم در برابر خوردگی استفاده می شود. برای کند کردن خوردگی محصولات فلزی در محیط اسیدی، از مواد خاصی - بازدارنده - نیز استفاده می شود.
زندگی و کار A.M. Butlerov
الکساندر باتلروف در سال 1828 در Butlerovka، یک روستای کوچک در نزدیکی کازان، جایی که املاک پدرش در آن قرار داشت، به دنیا آمد. ساشا مادرش را به یاد نمی آورد. ساشا که توسط پدرش، مردی تحصیل کرده بزرگ شده بود، می خواست در همه چیز مانند او باشد.
ابتدا به یک مدرسه شبانه روزی رفت و سپس وارد اولین سالن بدنسازی کازان شد که معلمان آن بسیار باتجربه و آماده بودند و می دانستند که چگونه دانش آموزان را علاقه مند کنند. ساشا به راحتی مطالب را یاد گرفت ، زیرا از اوایل کودکی به او آموزش داده شد که به طور سیستماتیک کار کند. او به ویژه جذب علوم طبیعی شد.
پس از فارغ التحصیلی از دبیرستان، برخلاف میل پدرش، ساشا وارد بخش علوم طبیعی دانشگاه کازان شد، اگرچه در حال حاضر فقط به عنوان دانشجو، زیرا او هنوز خردسال بود. تنها سال بعد، 1845، زمانی که این مرد جوان 17 ساله بود، نام او در لیست پذیرفته شدگان سال اول ظاهر شد.
در سال 1846، اسکندر به بیماری تیفوس مبتلا شد و به طور معجزه آسایی زنده ماند، اما پدرش که از او آلوده شده بود، درگذشت. در پاییز به همراه عمه خود به کازان نقل مکان کردند. به تدریج، جوانی عوارض خود را گرفت و سلامتی و تفریح ساشا بازگشت. باتلروف جوان با کوشش استثنایی مطالعه کرد، اما در کمال تعجب متوجه شد که بیشترین لذت را از سخنرانی های شیمی به او داده است. سخنرانی های پروفسور کلاوس او را راضی نکرد و او شروع به شرکت منظم در سخنرانی های نیکولای نیکولاویچ زینین کرد که برای دانشجویان گروه فیزیک و ریاضیات ارائه می شد. خیلی زود زینین، در حین تماشای اسکندر کار آزمایشگاهی، متوجه شد که این دانش آموز با موهای روشن استعداد غیر معمولی دارد و می تواند محقق خوبی شود.
باتلروف با موفقیت تحصیل کرد، اما به طور فزاینده ای به آینده خود فکر کرد، بدون اینکه بداند در نهایت باید چه چیزی را انتخاب کند. آیا می خواهید زیست شناسی بخوانید؟ اما، از سوی دیگر، عدم وجود یک ایده روشن است واکنش های آلیآیا امکانات بی پایانی برای اکتشاف ارائه نمی دهد؟
برای دریافت مدرک آکادمیک یک نامزد، باتلروف باید پس از فارغ التحصیلی پایان نامه ای ارائه می کرد. در این زمان زینین کازان را به مقصد سن پترزبورگ ترک کرده بود و چاره ای جز تحصیل در علوم طبیعی نداشت. باتلروف برای پایان نامه دکترای خود مقاله ای با عنوان "پروانه های روز جانوران ولگا-اورال" تهیه کرد. با این حال، شرایط به گونه ای بود که اسکندر هنوز مجبور بود به شیمی بازگردد.
پس از تصویب در شورا درجه علمیباتلروف برای کار در دانشگاه باقی ماند. تنها استاد شیمی، کلاوس، نمیتوانست تمام کلاسها را خودش تدریس کند و به یک دستیار نیاز داشت. باتلروف تبدیل به آن شد. در پاییز 1850 ، باتلروف امتحانات کارشناسی ارشد شیمی را گذراند و بلافاصله پایان نامه دکتری خود را با عنوان "در مورد روغن های ضروری"، که در ابتدا از آن دفاع کرد سال آینده. به موازات تهیه سخنرانی، باتلروف مطالعه دقیق تاریخ علم شیمی را آغاز کرد. دانشمند جوان در مطب، آزمایشگاه و خانه سخت کار کرد.
به گفته خاله هایش، آنها آپارتمان قدیمیتوپ ناراحت کننده بود، بنابراین آنها یکی دیگر، جادارتر را از سوفیا تیموفیونا آکساکوا، زنی پرانرژی و قاطع، اجاره کردند. او باتلروف را با مراقبت مادرانه پذیرفت و در او همتای مناسبی برای دخترش دید. الکساندر میخائیلوویچ علیرغم اشتغال مداوم خود در دانشگاه، فردی شاد و اجتماعی باقی ماند. او به هیچ وجه با «غیبت پروفسوری» بدنام متمایز نمی شد، و لبخند دوستانه و رفتار آسانش او را در همه جا مهمان پذیرایی می کرد. سوفیا تیموفیونا با رضایت خاطر نشان کرد که دانشمند جوان به وضوح نسبت به نادنکا بی تفاوت نبود. دختر واقعاً زیبا بود: پیشانی بلند و باهوش، چشمان درشت درخشان، ویژگیهای صورت دقیق و منظم و نوعی جذابیت خاص. جوانان دوستان خوبی شدند و با گذشت زمان به طور فزاینده ای نیاز به با هم بودن را احساس کردند و مخفی ترین افکار خود را به اشتراک گذاشتند. به زودی نادژدا میخایلوونا گلومیلینا، خواهرزاده نویسنده S.T. آکساکوا همسر الکساندر میخایلوویچ شد.
باتلروف نه تنها به عنوان یک شیمیدان برجسته، بلکه به عنوان یک گیاه شناس با استعداد نیز شناخته می شد. او آزمایش های مختلفی را در گلخانه های خود در کازان و بوتلرووکا انجام داد، مقالاتی در مورد مشکلات باغبانی، گلکاری و کشاورزی نوشت. او با حوصله و عشق کمیاب، رشد کاملیاهای ظریف و رزهای شاداب را تماشا کرد و انواع جدیدی از گلها را توسعه داد.
در 4 ژوئن 1854، باتلروف تأییدیه ای دریافت کرد که به او درجه علمی دکترای شیمی و فیزیک اعطا شده است. وقایع با سرعتی باورنکردنی رقم خوردند. باتلروف بلافاصله پس از دریافت مدرک دکترا به عنوان سرپرست استاد شیمی در دانشگاه کازان منصوب شد. در آغاز سال 1857 او قبلاً استاد شد و در تابستان همان سال اجازه سفر به خارج را دریافت کرد.
باتلروف در پایان تابستان وارد برلین شد. او سپس به تورهای آلمان، سوئیس، ایتالیا و فرانسه ادامه داد. مقصد نهایی سفر او پاریس، مرکز جهانی علوم شیمی در آن زمان بود. او قبل از هر چیز جذب ملاقاتش با آدولف ورتز شد. باتلروف دو ماه در آزمایشگاه ورتز کار کرد. در اینجا بود که او تحقیقات تجربی خود را آغاز کرد که طی بیست سال بعد با کشف ده ها ماده و واکنش جدید به اوج خود رسید. سنتزهای نمونه متعدد باتلروف از اتانول و اتیلن، الکل های سوم و پلیمریزاسیون هیدروکربن های اتیلن در منشأ تعدادی از صنایع قرار دارد و بنابراین، تأثیر تحریک کننده بسیار مستقیمی بر آن داشت.
باتلروف هنگام مطالعه هیدروکربن ها متوجه شد که آنها یک طبقه کاملاً ویژه را نشان می دهند مواد شیمیایی. با تجزیه و تحلیل ساختار و خواص آنها، دانشمند متوجه شد که یک الگوی دقیق در اینجا وجود دارد. این اساس نظریه ساختار شیمیایی او را تشکیل داد.
گزارش او در آکادمی علوم پاریس علاقه عمومی و بحث های پر جنب و جوشی را برانگیخت. باتلروف گفت: «شاید زمانی فرا رسیده است که تحقیقات ما باید مبنایی باشد نظریه جدیدساختار شیمیایی مواد این نظریه با دقت قوانین ریاضی متمایز می شود و به فرد امکان می دهد تا ویژگی ها را پیش بینی کند. ترکیبات آلی" هیچ کس تا کنون چنین افکاری را بیان نکرده است.
چند سال بعد، باتلروف در سفر دوم خود به خارج از کشور، نظریه ای را که برای بحث ایجاد کرده بود ارائه کرد. او در سی و ششمین کنگره طبیعت شناسان و پزشکان آلمانی در اسپایر گزارشی ارائه کرد. این کنگره در سپتامبر 1861 برگزار شد.
او به بخش شیمی ارائه کرد. عنوانی بیش از حد معمولی داشت: «چیزی در مورد ساختار شیمیایی اجسام».
باتلروف ساده و واضح صحبت کرد. او بدون پرداختن به جزئیات غیر ضروری، تئوری جدیدی را در مورد ساختار شیمیایی مواد آلی به مخاطبان معرفی کرد: گزارش او علاقه بی سابقه ای را برانگیخت.
اصطلاح "ساختار شیمیایی" قبل از باتلروف به کار رفته بود، اما او در مورد آن تجدید نظر کرد و از آن برای تعریف مفهوم جدیدی در مورد ترتیب پیوندهای بین اتمی در مولکول ها استفاده کرد. نظریه ساختار شیمیایی اکنون به عنوان پایه ای برای تمام شاخه های مدرن شیمی مصنوعی بدون استثنا عمل می کند.
بنابراین، این نظریه حق وجود خود را اعلام کرد. او خواستار شد توسعه بیشترو اگر در کازان نباشد، در کجای دیگر باید این کار انجام شود، زیرا نظریه جدیدی در آنجا متولد شد، خالق آن در آنجا کار کرد. برای باتلروف، وظایف رئیس جمهور بار سنگین و غیرقابل تحملی بود. او چندین بار درخواست کرد که از این سمت خلاص شود، اما همه درخواست هایش برآورده نشد. نگرانی او را هم در خانه رها نکرد. تنها در باغ، با مراقبت از گل های مورد علاقه اش، نگرانی ها و مشکلات روز گذشته را فراموش کرد. پسرش میشا اغلب با او در باغ کار می کرد. الکساندر میخائیلوویچ از پسر در مورد وقایع مدرسه پرسید و جزئیات جالبی در مورد گلها گفت.
سال 1863 فرا رسید - شادترین سال در زندگی دانشمند بزرگ. باتلروف در مسیر درستی قرار داشت. برای اولین بار در تاریخ شیمی، او موفق شد ساده ترین الکل سوم - الکل بوتیل سوم یا تری متیل کاربینول را به دست آورد. بلافاصله پس از این، گزارش هایی در مورد سنتز موفقیت آمیز بوتیل الکل های اولیه و ثانویه در ادبیات ظاهر شد.
دانشمندان ایزوبوتیل الکل را از سال 1852 می شناسند، زمانی که برای اولین بار از طبیعی جدا شد روغن نباتی. حالا دیگر بحثی وجود ندارد، زیرا چهار بوتیل الکل مختلف وجود داشت و همه آنها ایزومر بودند.
در سالهای 1862 - 1865، باتلروف موضع اصلی نظریه ایزومریزاسیون برگشت پذیر توتومریسم را بیان کرد، مکانیسم آن، به گفته باتلروف، شکافتن مولکول های یک ساختار و ترکیب بقایای آنها برای تشکیل مولکول هایی با ساختار متفاوت بود. ایده درخشانی بود. این دانشمند بزرگ نیاز به رویکرد پویا به فرآیندهای شیمیایی، یعنی در نظر گرفتن آنها را به عنوان تعادل، استدلال کرد.
موفقیت، اعتماد به نفس را برای دانشمند به ارمغان آورد، اما در عین حال او را با یک کار جدید و دشوارتر روبرو کرد. لازم بود تئوری ساختاری را برای همه واکنش ها و ترکیبات به کار برد شیمی آلیو مهمتر از همه، نوشتن یک کتاب درسی جدید در مورد شیمی آلی، که در آن همه پدیده ها از دیدگاه یک نظریه جدید ساختار در نظر گرفته شوند.
باتلروف تقریباً دو سال بدون وقفه روی کتاب درسی کار کرد. کتاب "مقدمه ای بر مطالعه کامل شیمی آلی" در سه نسخه بین سال های 1864 و 1866 منتشر شد. به هیچ وجه نمی شد آن را با هیچ یک از کتاب های درسی شناخته شده در آن زمان مقایسه کرد. این اثر الهام گرفته مکاشفه ای از باتلروف بود - یک شیمیدان، آزمایشگر و فیلسوف، که تمام مواد انباشته شده توسط علم را بر اساس یک اصل جدید و بر اساس اصل ساختار شیمیایی بازسازی کرد.
این کتاب یک انقلاب واقعی در علم شیمی ایجاد کرد. قبلاً در سال 1867، کار بر روی ترجمه و انتشار آن در سال 1395 آغاز شد آلمانی. به زودی پس از این، انتشارات تقریباً در همه رشته ها منتشر شد زبان های اروپایی. به گفته محقق آلمانی ویکتور مایر، تبدیل به " ستاره راهنما"در اکثریت قریب به اتفاق تحقیقات در زمینه شیمی آلی.
از زمانی که الکساندر میخائیلوویچ کار بر روی کتاب درسی را به پایان رساند، به طور فزاینده ای زمان خود را در Butlerovka گذراند. حتی در طول سال تحصیلیخانواده چندین بار در هفته به روستا می رفتند. باتلروف در اینجا احساس آزادی از نگرانی کرد و خود را کاملاً وقف سرگرمی های مورد علاقه خود کرد: گل ها و مجموعه حشرات.
اکنون باتلروف کمتر در آزمایشگاه کار می کرد، اما اکتشافات جدید را از نزدیک دنبال می کرد. در بهار سال 1868، به ابتکار شیمیدان مشهور مندلیف، الکساندر میخائیلوویچ به دانشگاه سن پترزبورگ دعوت شد، جایی که شروع به سخنرانی کرد و فرصتی یافت تا خود را سازماندهی کند. آزمایشگاه شیمی. باتلروف توسعه داد تکنیک جدیدآموزش دانشجویان، ارائه کارگاه آزمایشگاهی که در حال حاضر پذیرفته شده جهانی است، که در آن به دانش آموزان نحوه کار با انواع تجهیزات شیمیایی آموزش داده شد.
باتلروف در کنار فعالیت های علمی خود فعالانه درگیر است زندگی اجتماعیسن پترزبورگ در آن زمان جامعه مترقی به ویژه به موضوع آموزش زنان توجه داشت. زنان باید دسترسی آزاد داشته باشند آموزش عالی! دوره های عالی زنان در آکادمی پزشکی-جراحی سازماندهی شد، و کلاس ها در دوره های زنان Bestuzhev، جایی که باتلروف در مورد شیمی سخنرانی می کرد، شروع شد.
چند جانبه فعالیت علمیبوتلرووا از آکادمی علوم به رسمیت شناخته شد. در سال 1871 او به عنوان آکادمیک فوق العاده انتخاب شد و سه سال بعد - آکادمیک معمولی، که به او حق دریافت آپارتمان در ساختمان آکادمی را داد. نیکلای نیکولایویچ زینین نیز در آنجا زندگی می کرد. این نزدیکی باعث تقویت بیشتر دوستی دیرینه شد.
سالها به طور ناگزیر گذشت. کار با دانشجویان برای او بسیار دشوار شد و باتلروف تصمیم گرفت دانشگاه را ترک کند. او در 4 آوریل 1880 برای دانشجویان سال دوم سخنرانی خداحافظی کرد. خبر درگذشت استاد عزیزشان را با اندوه عمیق استقبال کردند. شورای دانشگاهی تصمیم گرفت از باتلروف بخواهد بماند و او را برای پنج سال دیگر انتخاب کرد.
دانشمند تصمیم گرفت فعالیت های خود را در دانشگاه فقط به خواندن درس اصلی محدود کند. و با این حال هفته ای چند بار در آزمایشگاه حاضر می شد و بر کار نظارت می کرد.
باتلروف در طول زندگی خود شور دیگری داشت - زنبورداری. او در ملک خود یک زنبورستان نمونه ترتیب داد و در سال های اخیرزندگی یک مدرسه واقعی برای زنبورداران دهقان است. باتلروف تقریباً به کتاب خود "زنبور، زندگی آن و قوانین زنبورداری هوشمند" افتخار می کرد تا آثار علمی خود.
باتلروف معتقد بود که یک دانشمند واقعی باید علم خود را نیز رواج دهد. او به موازات مقالات علمی، بروشورهایی را منتشر می کرد که در دسترس عموم بود و در آنها به روشنی و رنگارنگ درباره اکتشافات خود صحبت می کرد. او آخرین آنها را شش ماه قبل از مرگش به پایان رساند.
رسیدن به هر هدفی کار روزانه است. اگر هدف شما دریافت است برداشت خوب، پس نه تنها باید نیروی کار خود را سرمایه گذاری کنید، بلکه باید باغ و باغ سبزی خود را نیز با مراقبت، توجه و مراقبت مناسب تهیه کنید. قطعا یک تجربه چندین سالاو به همه یاد داد که وقتی هر چیزی را در باغ پرورش می دهید، نمی توانید بدون مواد شیمیایی کار کنید.
به احتمال زیاد، همه در مورد آهک خاموش در یک منطقه گفتگو یا دیگری شنیده اند. آهک خاموش (یا همانطور که به آن کرک نیز گفته می شود) یک نام شیمیایی دارد - هیدروکسید کلسیم. جالب است که از چنین آهکی در زمینه های مختلف استفاده می شود: ساختمان سازی، نرم کننده آب، دباغی چرم، دندانپزشکی، صنایع شیمیایی. در باغبانی نیز استفاده شده است.
ترکیب آهک خشک شده کاملاً ساده است، اکسیدهای کلسیم در آن غالب است. فرآیند به دست آوردن (کوئنچ) نیز پیچیده نیست و شامل اضافه کردن آب و مخلوط کردن کامل است.
تهیه آهک خشک شده (کرک) برای انجام این کار دشوار نیست، باید آن را با آب خاموش کنید (مخلوط کنید) که حدود 10-20 دقیقه طول می کشد. در طی فرآیند خاموش کردن، کود دهی سالم و ایمن انجام می شود.
قاعده اصلی این است که آب آبکش باید سرد باشد تا آهک مواد مفید خود را از دست ندهد.
استفاده از آهک خشک شده در باغبانی بسیار گسترده است. یک روش ساده و بی تکلف مدتهاست که به یکی از ابزارهای اصلی تبدیل شده است باغبان باتجربه. برخی از روش های کاربردی:
- کنترل علف های هرز: برخی از انواع علف های هرز را می توان به طور کامل از باغ حذف کرد دوره پاییزآهک زدن خاک میزان کاربرد - 300-400 گرم در هر متر مربع. پس از عمل، از علف های هرز نمی ترسید: دم اسب، علف گندم، شپش چوب، ترشک اسب.
- همچنین می توان به آن آهک خرد شده اضافه کرد گودال کمپوست- به این ترتیب فرآیند تجزیه محتویات آن را تسریع خواهید کرد.
- اکسید زدایی خاک با استفاده از آهک نیاز به رعایت هنجارها و دوزها دارد: خاک های سنگین و رسی - 600-900 گرم. در هر متر مربع، سبک، لومی - 400-500 گرم. در هر متر مربع متر، سبک، شنی - 300-400 گرم. در هر متر مربع آهک گذاری خاک هر 3-4 سال یک بار انجام می شود.
- فرآیند سفید کردن درختان بسیار ساده است. استفاده از آهک درجه یک یا درجه یک توصیه می شود. آهک را رقیق کنید تا یک رنگ سفید غنی بدست آورید، نسبت تقریبی آن 1:1 است.
تفاوت بین آهک خرد شده و زنده
منطقی است که فکر کنیم اگر آهک ژولیده وجود دارد، پس باید آهک زنده وجود داشته باشد. تفاوت آن با slaked چیست و کجا استفاده می شود؟ مهم نیست که چقدر متناقض به نظر می رسد، کلمه "آهک" ریشه یونانی دارد و به معنای "خفه نشدنی" است.
آهک زنده ظاهری دانه ای دارد. قبلاً می شد از آهک زنده استفاده کرد کار ساخت و سازبه عنوان سیمان، با این حال، در نتیجه این کاربرد، متوجه شد که اینطور نیست بهترین خواصیعنی جذب رطوبت و تکثیر کپک قارچی. با وجود این، آهک زنده به طور گسترده در ساخت و ساز برای تولید بتن سرباره، رنگ، آجر ماسه آهکی و مواد گچ استفاده می شود. در صنایع غذایی، آهک زنده به عنوان یک امولسیفایر عمل می کند و به اتصال موادی که خواص آنها اجازه حل شدن در یکدیگر را نمی دهد، کمک می کند. آهک زنده همچنین در فرآیند خنثی سازی فاضلاب و گازهای دودکش استفاده می شود.
تفاوت اصلی بین آهک خرد شده و زنده در فرمول شیمیایی آن است. آهک خشک شده هیدروکسید کلسیم است و آهک زنده اکسید کلسیم است. آهک زنده بر خلاف آهک خشک شده که اغلب به صورت پودر یافت می شود، دانه ای است.
قوانین کاهش آهک و اقدامات احتیاطی ایمنی
کم آبی فرآیندی است که آهک را از بین می برد. قبل از شروع کار با آهک، مطمئن شوید که تمام اقدامات ایمنی را رعایت کنید:
- لباس شما باید تنگ باشد، با دستکش، ماسک تنفسی و عینک ایمنی کار کنید.
- خاموش کردن باید منحصراً در یک ظرف فلزی انجام شود.
- اگر خاموش کردن در داخل خانه انجام می شود، از تهویه خوب اطمینان حاصل کنید.
- اگر آهک وارد چشم یا پوست شما شد، باید ناحیه آسیب دیده را با محلول سرکه ضعیف یا آب فراوان بشویید و سپس با پزشک مشورت کنید.
آبگیری در فضای باز انجام می شود. با توجه به سرعت انقراض آنها متمایز می شوند:
- آهک خاموش کننده سریع - تا 8 دقیقه؛
- آهک با شل شدن متوسط - تا 25 دقیقه؛
- آهک آرام آرام - بیش از 25 دقیقه.
فرآیند slaking افزودن آب به آهک زنده است. افزودن آب باید به آرامی انجام شود تا دما کاهش نیابد، زیرا در طی فرآیند خاموش کردن گرما آزاد می شود.
آهک باید تحت شرایط خاصی ذخیره شود. یک گودال برای ذخیره سازی آماده کنید، محلول را با یک لایه ماسه 20 سانتی متری روی آن بپاشید (اگر انتظار می رود ذخیره سازی در یخبندان باشد، می توان یک لایه 50-70 سانتی متری زمین را روی ماسه اضافه کرد). برای ایمنی مردم و حیوانات گودال را حصار بکشید.
ویژگی های استفاده از کرک در باغ
آهک آب شده یک ماده آلی است. عناصر اصلی کرک کلسیت و دولومیت هستند. همانطور که قبلاً ذکر شد، آهک خرد شده را می توان به عنوان کود و به عنوان استفاده کرد عامل محافظدر باغ و سبزی.
کرک سرشار از پتاسیم، منیزیم و کلسیم است و به سرعت در باغبانی محبوبیت پیدا کرده است. علاوه بر این، پتاسیم موجود در ترکیب دارای شکلی است که به سرعت توسط گیاهان جذب می شود. کلسیم باید جزئی از خاک باشد، مسئول ایمنی گیاه، محافظت در برابر بیماری ها است، بنابراین آهک خرد شده مقرون به صرفه است و گزینه موثربرای پر کردن خاک با کلسیم کلسیم علاوه بر اثر مستقیم، فعالیت میکروارگانیسم ها را فعال می کند و آنها شروع به ترشح نیتروژن می کنند. استفاده از کرک باعث تغییر می شود ترکیب شیمیاییخاک، عادی سازی و کسب آن توابع لازمو اجزاء
محبوب ترین و مواد عملیکه کاربرد وسیعی در ساخت و ساز، تعمیرات، کشاورزی و زندگی روزمره پیدا کرده است، آهک خشک شده است.
این جزء اصلی پوشش های مدرن، مخلوط ها و محلول های با بالا است ویژگی های عملکرد. در مورد نحوه صحیح خرد کردن و ذخیره آهک و همچنین برای اهدافی که می توان از آن استفاده کرد، بیشتر بخوانید.
آهک خاموش یک ترکیب شیمیایی پودری به شکل معدنی (Ca(OH) 2) است که از برهمکنش اکسید کلسیم به دست می آید. آهک زنده) و آب.
هنگام تولید آهک هیدراته، حفظ صحیح آن مهم است رژیم دماآب گرم کن، که نباید بیش از 500 درجه باشد. هر چه دمای آب بالاتر باشد، کیفیت محصول نهایی پایین تر است.
بسته به روش خاموش کردن، انواع ترکیبات زیر را می توان تشکیل داد:
- آب آهک.
- شیر آهک (تعلیق).
- خمیر آهک.
- فلاف (هیدروکسید کلسیم به صورت پودر).
تفاوت بین آهک خرد شده و زنده
تفاوت بین آهک خرد شده و زنده در فرمول شیمیایی و خواص ماده نهفته است.
ویژگی های متمایز این دو ماده به وضوح در جدول ارائه شده است.
شما می توانید آهک را از مواد اولیه نه تنها از نظر بصری، بلکه از نظر لمسی نیز تشخیص دهید - قادر به رهاسازی نیست. انرژی حرارتی، بنابراین همیشه سرد می ماند.
آهک زنده سنگی است که از سوزاندن سنگ های گچ یا سنگ آهک در دمای بالای 1000 درجه به دست می آید. به دلیل رطوبت سنجی بالا، این ماده به ندرت به شکل خالص خود استفاده می شود. برای تهیه انواع مختلف طراحی شده است خمپاره ها، مخلوط ها و عناصر.
دستورالعمل های آهک زدایی
فرآیند کاهش آهک را می توان در محل ساخت و ساز یا در خانه سازماندهی کرد. بسته به نوع ماده اولیه، محلول نهایی عبارت است از:
- اطفاء سریع (در 10 دقیقه پخته می شود).
- اطفاء متوسط (خاموش در 25 دقیقه).
- پخت آهسته (حداکثر 1 ساعت طول می کشد تا بپزد).
مدت زمان کوئنچ با زمان از شروع افزودن آب به ماده اولیه تا زمانی که ترکیب شیمیایی محصول نهایی به طور کامل تثبیت شود تعیین می شود.
مرحله مقدماتی
برای کار لازم است مواد اولیه و وسایل تهیه شود حفاظت شخصیاز تاثیر منفیبخار حرارتی - دستکش، عینک، ماسک، لباس ساخته شده از پارچه ضخیم.
ماده اولیه باید آهک به شکل آهک زنده، چوبی عمیق یا ظرف فلزیو دستگاه خمیر زنی
همچنین، برای تهیه حجم زیادی از مخلوط به یک گودال خاکی و یک جعبه بزرگ ساخته شده از آن نیاز دارید پایه چوبی، مجهز به پنجره تخلیه با فیلتر توری.
فرآیند خاموش کردن
برای به دست آوردن آهک هیدراته با کیفیت بالا مراحل زیر انجام می شود:
- مواد اولیه در ظرف آماده شده ریخته می شود.
- آب به تدریج به نسبت 1:1 به پایه اضافه می شود و به آرامی هم می شود تا فرآیند خاموش شدن فعال شود. این نسبت برای تهیه کرک - مخلوط پودری - مناسب است. برای به دست آوردن خمیر یا شیر آهک باید 400 گرم آب به 1 کیلوگرم مواد اولیه اضافه کرد.
- هم زدن ماده تا زمانی که واکنش کوئنچ به طور کامل کامل شود انجام می شود.
- محلول تازه از بین رفته به مدت 40 ساعت در ظرفی دم میشود تا غلیظ شود و 30 روز پس از آمادهسازی استفاده میشود.
لغو در جعبه چوبی
اگر از جعبه چوبی برای تهیه آهک استفاده می شد، مخلوط آمادهآن را از طریق یک پنجره فیلتر به یک گودال خاکی تخلیه می کنند، با تخته پوشانده می شود و برای چند روز تزریق می شود.
پس از پایان دوره، آهک با یک لایه ماسه به ارتفاع 18 سانتی متر پوشانده می شود و به مدت 2 تا 3 هفته دم می شود.
قوانین نگهداری آهک
آهک هیدراته یک محصول ذخیره سازی طولانی مدت است که ساختار شیمیایی خود را تغییر نمی دهد و از بین نمی رود خواص مفیددر طول کل عمر سرویس
- پس از اتمام آبگیری، مدت زمان قرار گرفتن در معرض مواد: برای تهیه ملات و عناصر - 2 هفته، برای گچ کاری - 30 روز.
- در ذخیره سازی زمستانیمواد در گودال، یک بالشتک عایق حرارتی اضافی نصب شده است: تا 20 سانتی متر ماسه و 70 سانتی متر خاک نیز می توانید از عایق جامد استفاده کنید.
- نگهداری مواد در بسته بندی ها در شرایط تهویه مناسب مجاز است انبارهابا بتن، آسفالت و کف های آجری. انبارها باید تجهیزات ایمنی آتش نشانی لازم را داشته باشند: جعبه های چوبیبا ماسه، کپسول های آتش نشانی با دی اکسید کربن، شیرهای آتش نشانی با شیلنگ های هیدرولیک.
- آهک خشک شده نباید در نزدیکی مواد منفجره یا قابل اشتعال نگهداری شود.
به دلیل ویژگی های منحصر به فردش، آهک ژولیده از دیرباز مورد استفاده قرار می گرفته است ساخت و ساز مدرن، پزشکی، باغبانی و زندگی روزمره.
کاربرد در ساخت و ساز
استفاده گسترده از آهک در ساخت و ساز برای حل مشکلات زیر:
- سفید کاری داخلی سطوح داخلی.
- تهیه ملات، مخلوط اتصال و ترکیبات رنگی.
- حفاظت سازه های چوبیاز آتش و پوسیدگی
- تولید بتن چوبی، بلوک خاکستر، بلوک آجر سیلیکات و بتن سنگین.
- تهیه ترکیب بنایی برای ساخت سازه های کوره.
- تولید ملات سیمان آهکی.
- تهیه آب آهک برای تعیین ترکیبات دی اکسید کربن.
ویژگی های هیدرولیک سخت شدن سریع ملات های آماده بر اساس آهک را تضمین می کند. بنابراین، آنها اغلب در ساخت عناصر پشتیبان پل ها و سایر سازه های با پیچیدگی افزایش یافته استفاده می شوند.
در زندگی روزمره استفاده کنید
چند راه برای استفاده از مواد در خانه:
- تهیه کودهای بی خطر برای کاهش اسیدیته خاک و کنترل آفات مختلف.
- تهیه محلول پیشگیرانه برای سفیدکردن تنه درختان باغی و زینتی.
- تهیه مخلوط هایی برای محافظت از گیاهان در برابر بیماری های قارچی، حشرات و جوندگان کوچک.
- تهیه یک افزودنی فعال برای تغذیه پرندگان و حیوانات.
- سختی کاهش یافته است آب آشامیدنیاز چاه، چاه و تامین آب.
- ضد عفونی و ضد عفونی سطوح مختلفو سازه های چوبی
- سوزاندن کربنات سدیم یا پتاسیم.
- خنثی سازی ترکیبات اسیدی و اسیدهای آلی.
- دباغی و فرآوری چرم طبیعی.
- تهیه مکمل های غذایی. رایج ترین آنها امولسیفایر (E526) است.
یک ماده منحصر به فرد که دارای مزایای زیر است: آماده سازی آسان، ماندگاری، ویژگی های ضد عفونی عالی، طیف وسیعی از کاربردها. و یادگیری فرآیند کندن آهک در خانه بسیار آسان است. راه حل های آماده با موفقیت برای کارهای کشاورزی استفاده می شود. تعمیرات خانگی، ساخت ساختمان های مسکونی و تجاری که در درجه اول به دلیل هزینه پایین مواد اولیه مصرفی می باشد.
آهک یک کلمه یونانی است که معنای خاص خود را دارد. ترجمه تحت اللفظی آن به معنای «خفه نشدنی» است. این یکی از آن موادی است که از زمان های بسیار قدیم وجود داشته است. بشریت برای مدت طولانی از آن برای اهداف خود استفاده کرده است. به اندازه کافی عجیب، خواص آن کاملاً تصادفی مشخص شد. اما آنها شروع کردند به استفاده از مطالب در بسیاری از زمینه ها، از طریق خطاها و آزمایشات، کورکورانه. آهک یک ماده همه کاره است که هنوز هم استفاده می شود.
این ماده به دلیل خواصی که دارد در صنایع مختلفی استفاده می شود که با یکدیگر متفاوت هستند. در این مقاله به نحوه استخراج مواد، تفاوت آهک خشک شده با آهک زنده و در چه مناطقی از آن استفاده می شود، خواهیم پرداخت.
تاریخچه مواد
در زمان های قدیم، زمانی که مردم هنوز چیزی در مورد کلسیم و ترکیبات آن با اکسیژن و زغال سنگ نمی فهمیدند، متوجه چیزی می شدند. دقیقا چی؟ از طریق "پوکینگ علمی" مشخص شد که سنگ آهک دارای خواص عالی است، به ویژه به عنوان مصالح ساختمانی. علاوه بر این، اگر برخی از سنگ ها مانند سنگ آهک، دولومیت، گچ و غیره را بسوزانید، ماده ای به دست می آید که خاصیت اتصال دارد.

اگر داستان را به خاطر داشته باشید چین باستان، سپس کارگران خاک را با سیمان آهکی تثبیت کردند و سنگ تراشی بزرگ معروف خود را چیدند دیوار چینی. طول آن 2500 کیلومتر است. نکته شگفت انگیز این است که تا به امروز باقی مانده است و امروز می توانیم به عظمت آن فکر کنیم. با گذشت زمان، آهک به یک جزء کلیدی در تهیه کودهای مورد استفاده در کشاورزی تبدیل شده است.
دو نوع ماده وجود دارد: آهک خرد شده و آهک زنده. این یا آن نوع چگونه به دست می آید؟ چه تفاوتی بین آنها وجود دارد؟ بیایید پاسخ این سوالات را دریابیم.
تولید مواد اولیه
ما قبلاً می دانیم که آهک محصول سنگ است. استخراج آن با پخت در کوره های مخصوص ساخته شده از سنگ آهک، دولومیت و گچ انجام می شود. خروجی مواد به شکل توده های سفید یا همانطور که به آن می گویند - توده "جوش" است. این آهک زنده است. فرآیند استخراج در کارخانه های ویژه انجام می شود که آهک از آنجا بیشتر منتقل می شود. "کیپلکا" محصول اولیه ای است که انواع دیگر از آن تولید خواهد شد. فرمول شیمیاییمواد - CaO (اکسید کلسیم).

ماده اولیه آماده پس از پخت، برای ملات و سیمان استفاده نمی شود، زیرا توانایی جذب رطوبت بسیار قوی را دارد و همچنین به تشکیل کپک قارچی روی دیوارها کمک می کند. با این حال، آب جوش بسیار مورد تقاضا است صنعت ساخت و ساز، یعنی برای تولید بتن سرباره، آجر شن و ماسه آهک، رنگ و مخلوط برای گچ.

بسته به مدت زمان خاموش کردن توده "جوش" به 3 نوع تقسیم می شود. اولین آنها آهک زودباخته است. مدت زمان لازم برای بازپرداخت آن تا 8 دقیقه است. نوع دوم خاموش کننده متوسط است که در 25 دقیقه می رسد. خوب، نوع آخر، آهسته خاموش است، که برای رسیدن به شرایط به 25 دقیقه یا بیشتر نیاز دارد. بنابراین ما به آرامی به سراغ نوع دیگری از مواد رفتیم - آهک خاموش.
آهک خرد شده
تفاوت بین آهک خشک شده و زنده چگونه بیان می شود؟ خود نام قبلاً نشان می دهد که تفاوت بین مواد چیست. اگر ماده خام معمولی دارای فرمول CaO باشد، پس از افزودن آب، ماده خاموش شده به دست می آید: CaO + H 2 O = Ca(OH) 2. این روند انقراض است. قابل ذکر است که وقتی مواد اولیه با آب مخلوط می شود، واکنش شدیدی رخ می دهد که مقدار زیادی گرما و دود آزاد می کند. آب به معنای واقعی کلمه در حال جوشیدن است. به همین دلیل به آهک کلوخه «آهک جوشان» می گویند. خروجی کرک هیدراته است.

از کلوخه "دیگ" می توانید انواع مختلفی را دریافت کنید: آهک زنده آسیاب شده، کرک هیدراته، خمیر سنگ آهک یا شیر. بسته به مقدار آب اضافه شده برای کوئنچ، خمیر یا شیر به دست می آید. به عنوان مثال، برای به دست آوردن خمیر سنگ آهک، مایع واکنش 3-4 برابر بیشتر از خود ماده نیاز دارد. و اگر نیاز به شیر سنگ آهک دارید، مقدار مایع 8-10 برابر افزایش می یابد.

نحوه تولید کرک شل شده
برای تولید آهک خشک شده، باید قوانینی را رعایت کنید. کم آبی (فرایند کوئنچ) باید در هوای آزاد انجام شود. خود مواد اولیه باید در یک مخزن یا ظرف قرار داده شوند. از آنجایی که مقدار زیادی بخار در طول فرآیند آزاد می شود، باید از خود محافظت کنید. خود این ماده نیز می تواند به انسان آسیب برساند و حتی پوست را بسوزاند. به همین دلیل محافظت از پوست دست و کل بدن، چشم ها و مجاری تنفسی ضروری است. شما نمی توانید بدون کت و شلوار یا لباس مخصوص، دستکش، عینک و ماسک تنفسی کار کنید. سپس همه چیز برای سلامتی شما بی خطر خواهد بود.
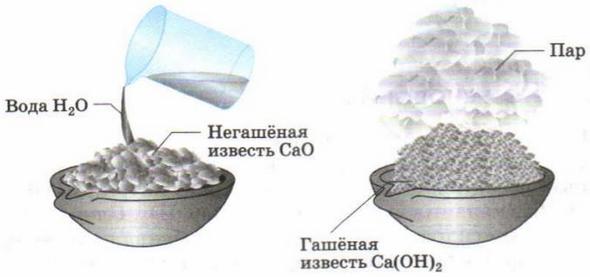
لازم به یادآوری است که در این مورد نیازی به عجله نیست. کیفیت آهک زنده می تواند متفاوت باشد، برخی به سرعت کم می شوند، برخی دیگر زمان زیادی می برد. اگر تمام کار را کامل نکنید، ممکن است مواد در گچ تمام شده دود شود. هنگامی که از آهک کند کنده استفاده می کنید، توصیه نمی شود فوراً آن را با آب پر کنید. بهتر است این کار را در قسمت های کوچک انجام دهید. خاموش کننده متوسط و سریع تا زمانی که بخار به طور کامل ناپدید شود برای جلوگیری از فرسودگی ریخته می شود.
توجه کن!آهک تازه از بین رفته ممکن است دارای بقایای مواد اولیه باشد. آنها دوباره خاموش می شوند و سپس خارج می شوند.
پس از آبگیری میزان آهک بیشتر می شود. از 1 کیلوگرم آهک زنده می توانید 2 یا بیشتر بدست آورید. آهک خرد شده و تفاوت برجستهآشکار است. اما این مواد کجا استفاده می شوند؟
کاربرد در ساخت و ساز
عمده ترین منطقه ای که در آن از آهک خشک شده و زنده استفاده می شود ساختمان سازی است. آهک فوق العاده است مواد چسباننده. یکی از مزایای آن سازگاری با محیط زیست و طبیعی بودن آن است. برای انسان کاملا بی ضرر است. قبلاً کمی در مورد استفاده از مواد خام آهک زنده صحبت کرده ایم، اما اینها همه جنبه ها نیستند. برای تولید مخلوط ساختمانی خشک، ملات و ترکیب گچ لازم است. علاوه بر این، با افزودن آهک به محصولات بتنی، آنها بسیار قوی تر، مقاوم تر در برابر رطوبت و متراکم تر می شوند.
